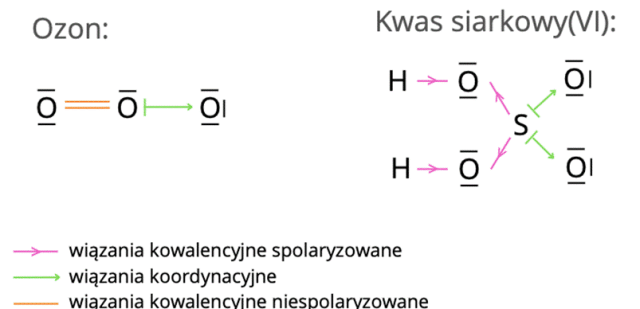

Wiązanie koordynacyjne to takie, w którym para elektronów wiązaniu pochodzi od tylko jednego atomu. Dawca pary to donor (tu: tlen w cząsteczce ozonu, siarka w cząsteczce kwasu), a biorca to akceptor (tu: tlen w obu cząsteczkach). Donor musi mieć utworzoną trwałą konfigurację elektronową i dodatkową wolną parę elektronów, by przekazać ją akceptorowi.
W cząsteczce ozonu: Pomiędzy dwoma atomami tlenu tworzą się dwa wiązania kowalencyjne niespolaryzowane. W ten sposób oba atomy tlenu uzyskują oktet elektronowy. Jeden z atomów tlenu może zostać donorem wolnej pary elektronowej, by trzeci atom tlenu również miał oktet. Wolna para elektronowa ulega uwspólnieniu.
W cząsteczce kwasu: Pomiędzy atomami wodoru i tlenu oraz tlenu i siarki tworzą się wiązania kowalencyjne spolaryzowane. Wodór uzyskuje dublet elektronowy, a atomy tlenu i siarki – oktet. W ten sposób siarka może stać się donorem wolnych par elektronowych dla atomów tlenu. Wolna para elektronowa ulega uwspólnieniu.