Na2S (siarczek sodu) — wiązania jonowe
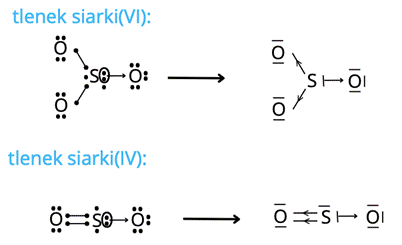
SO2 (tlenek siarki (IV)) — wiązania kowalencyjne spolaryzowane i wiązanie koordynacyjne
SO3 (tlenek siarki (VI)) — wiązania kowalencyjne spolaryzowane i wiązanie koordynacyjne

Rodzaj wiązania zależy od różnicy elektroujemności w cząsteczkach. Wartości elektroujemności zawarte są w układzie okresowym. Siarczek sodu utworzony jest przez metal oraz niemetal – stąd między tymi pierwiastkami tworzy się wiązanie jonowe. Atom sodu (każdy z osobna) oddaje elektron atomowi siarki. Pozwala to wszystkim atomom na osiągnięcie korzystnej konfiguracji elektronowej.
Elektroujemności atomów O oraz S wynosi kolejno: 3,5 oraz 2,5. Stąd różnice elektroujemności w związkach to:
elektroujemność tlenu – elektroujemność siarki = 3,5 – 2,5 = 1
Elektroujemność w zakresie od 0,4 do 1,7 wskazuje na wiązanie kowalencyjne spolaryzowane. Szczególnym typem takiego wiązania jest wiązanie koordynacyjne. Wiązania w tlenkach siarki tworzą się zgodnie z powyższymi schematami.