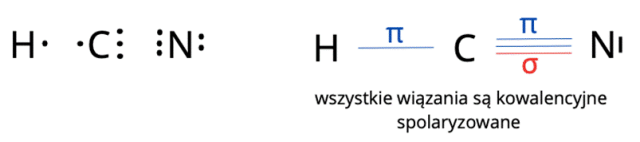

W pierwszej kolejności zapisz wzory elektronowe. Przedstawiają one rozmieszczenie elektronów na atomach. Liczba elektronów walencyjnych różni się dla każdego z atomów, ale często odpowiada ona numerowi grupy lub w przypadku pierwiastków w grupach 11-18 – cyfrze jedności. Węgiel ma cztery elektrony walencyjne, wodór jedno, a azot pięć. Stąd do oktetów elektronowych (do których dążą) brakuje im kolejno czterech, jednego oraz trzech elektronów walencyjnych.
Atom węgla jedno wiązanie kowalencyjne spolaryzowane z atomem wodoru. Jest one spolaryzowane ze względu na różnicę elektroujemności wynoszącą 0,4:
różnica elektroujemności = elektroujemność atomu węgla – elektroujemność atomu wodoru = 2,5 – 2,1 = 0,4
Również pomiędzy atomem węgla a atomem azotu tworzą się wiązania kowalencyjne spolaryzowane, ponieważ ich różnica elektroujemności wynosi 0,5:
różnica elektroujemności = elektroujemność atomu azotu – elektroujemność atomu węgla = 3,0 – 2,5 = 0,5
Wiązanie typu sigma to wiązanie, które tworzy się jako pierwsze. Kolejne wiązanie w wiązaniu wielokrotnym to wiązanie pi. Zatem wiązaniu pi zawsze towarzyszy wiązanie sigma. Wiązanie pomiędzy węglem a wodorem jest pojedyncze – jest to w związku z tym wiązanie sigma. Pomiędzy węglem a azotem powstają trzy wiązania – jedno wiązanie sigma i dwa pi.