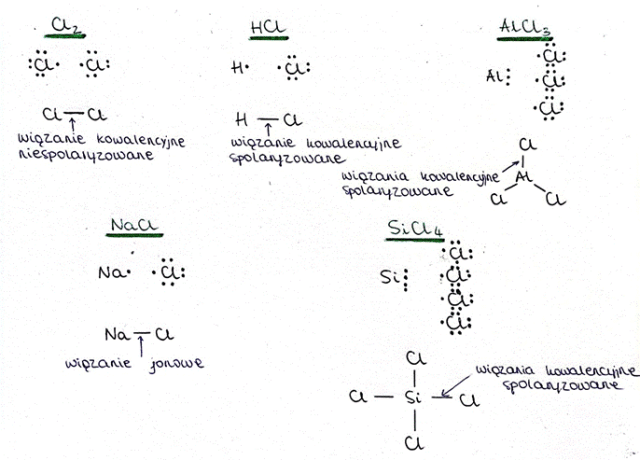

Najpierw zapisz wzory elektronowe Lewisa. Są to takie wzory, które przedstawiają schematycznie rozmieszczenie elektronów walencyjnych jako kropek. Liczba elektronów walencyjnych różni się dla każdego z atomów, ale często odpowiada ona numerowi grupy lub w przypadku pierwiastków w grupach 11-18 – cyfrze jedności.
Wzory strukturalne przedstawiają tylko wiązania – nie zaznaczamy polaryzacji czy wolnych par elektronowych.
Aby ustalić rodzaj wiązań, w pierwszym kroku spójrz do tablicy pierwiastków chemicznych. Wiązania w substancjach można określić na podstawie różnic elektroujemności pomiędzy atomami. Jeśli różnica wynosi poniżej 0,4 – jest to wiązanie kowalencyjne niespolaryzowane (inaczej atomowe). Jeśli ta różnica wynosi powyżej 1,7 – mówimy o wiązaniu jonowym. Wartości pośrednie sugerują wiązanie kowalencyjne spolaryzowane.