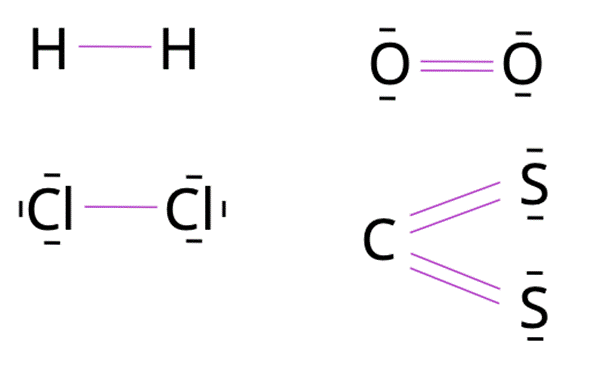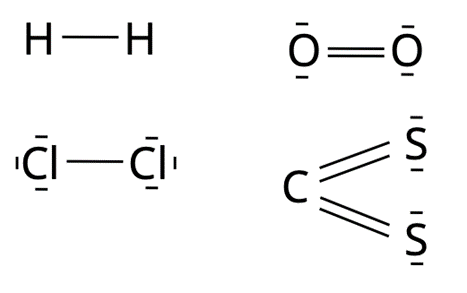

W pierwszym kroku spójrz na wzory cząsteczek. Wszystkie atomy dążą do uzyskania konfiguracji elektronowej gazu szlachetnego, czyli do posiadania dwóch lub ośmiu elektronów. To, ilu elektronów brakuje im do dubletu lub oktetu warunkuje ilość tworzonych wiązań. Elektron ten może zostać uwspólniony pomiędzy atomami, co powoduje powstanie wiązania. Elektrony walencyjne, które nie biorą udziału w wiązaniu, tworzą pary niewiążące (dwa elektrony to jedna para). Fioletowe kreski symbolizują wiązania pomiędzy elektronami wiążącymi. Czarne kreski to wolne pary elektronowe. Liczba elektronów walencyjnych różni się dla każdego z atomów, ale często odpowiada ona numerowi grupy lub w przypadku pierwiastków w grupach 11-18 – cyfrze jedności.