

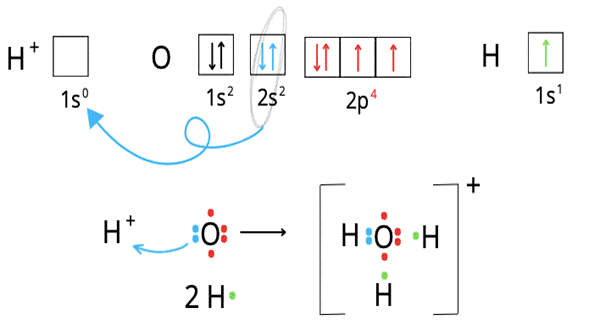
Wiązanie koordynacyjne to takie, w którym para elektronów wiązaniu pochodzi od tylko jednego atomu. Dawca pary to donor (tu: tlen), a biorca to akceptor (tu: wodór). Donor musi mieć utworzoną trwałą konfigurację elektronową i dodatkową wolną parę elektronów, by przekazać ją akceptorowi.
Atom wodoru ma jeden elektron walencyjny, atom tlenu – sześć.
Atom tlenu tworzy dwa wiązania kowalencyjne spolaryzowane z atomami wodoru. Stąd uzyskuje dodatkowe dwa elektrony, które uwspólnia.
W związku z tym ma ich w sumie tyle, by zapełnić całą podpowłokę 2p. Może zatem oddać elektrony z podpowłoki 2s kolejnemu atomowi wodoru. W ten sposób powstaje kation hydroniowy o wzorze sumarycznym H3O+.
Elektrony poszczególnych atomów zaznaczono na ilustracji przy pomocy kolorowych strzałek oraz schematycznych kropek.