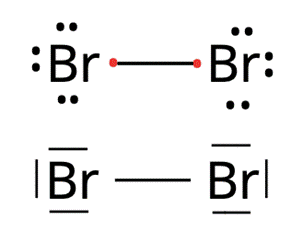
W cząsteczce Br2 występuje wiązanie kowalencyjne niespolaryzowane (atomowe).

W pierwszym kroku zapisz wzór cząsteczki bromu – Br2. Brom ma siedem elektronów walencyjnych. Do uzyskania oktetu elektronowego brakuje mu jednego elektronu. Elektron ten może zostać uwspólniony pomiędzy atomami bromu, co powoduje powstanie wiązania kowalencyjnego niespolaryzowanego. Elektrony walencyjne, które nie biorą udziału w wiązaniu tworzą pary niewiążące (dwa elektrony to jedna para). Na czerwono zaznaczono elektrony wiążące, a na czarno – niewiążące. Czarne kreski to pary elektronów niewiążących. Jest ich sześć.