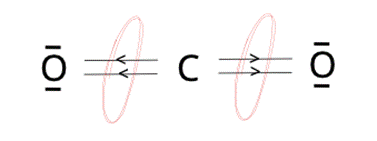Moment dipolowy wykazują: H2O, H2S, NH3.

Moment dipolowy to taka wartość fizyczna, która jest charakterystyczna dla związków z wiązaniem kowalencyjnym spolaryzowanym. Wynika z różnicy elektroujemności i przesunięcia pary elektronowej do atomu pierwiastka bardziej elektroujemnego. Wszystkie spośród związków wymienionych w zadaniu mają wiązania kowalencyjne spolaryzowane. Jednak niektóre związki, mimo takich wiązań, nie wykazują momentu dipolowego. Wynika to z tego, że momenty dipolowe części wiązań równoważą się ze sobą przez przeciwne zwroty. Jest tak między innymi w takich związkach jak: CO2, CCl4 czy SiF4. W cząsteczce dwutlenku węgla przedstawia się to następująco: