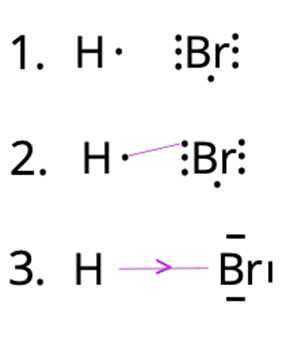

W pierwszym kroku spójrz na wzór cząsteczki – HBr. Zapisz elektrony walencyjne – jeden dla wodoru i siedem dla bromu. Następnie połącz elektrony tak, by atomy wodoru miały ich po dwa, atom bromu – osiem. Powstaną w ten sposób dwa wiązania. Są one kowalencyjne spolaryzowane, ponieważ elektroujemność wodoru wynosi 2,1, a bromu – 2,8. Różnica wynosi zatem 0,7. Jeśli różnica wynosi poniżej 0,4 – jest to wiązanie kowalencyjne niespolaryzowane (inaczej atomowe). Jeśli ta różnica wynosi powyżej 1,7 – mówimy o wiązaniu jonowym. Wartości pośrednie sugerują wiązanie kowalencyjne spolaryzowane. Na końcu zapisz wolne pary elektronowe na atomie bromu – są to te elektrony, które nie brały udziału w tworzeniu wiązania.