W tym zadaniu oblicz masę tlenu O2 pod ciśnieniem p1 = 15 MPa w temperaturze T1 = 27oC znajdującego się w butli o pojemności V = 2 l. Stała gzowa ![]()
Korzystamy z równania Clapeyrona:
![]()
Liczbę moli w równaniu wyrażamy jako iloraz masy gazu do masy molowej ![]()
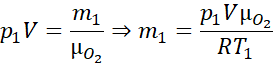
Temperaturę przeliczamy na kelwiny ![]()
![]()
Wstawiamy wartości liczbowe, wyrażone w jednostkach SI:
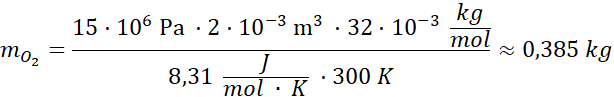
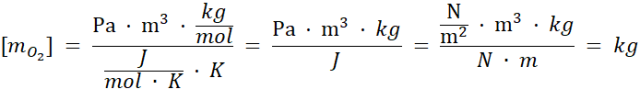
Odpowiedź: Masa tlenu w butli wynosi ok. 0,385 kg.

Korzystamy z równania Clapeyrona, gdzie liczbę moli wyrażamy jako iloraz masy gazu do masy molowej. Poprawność wzoru sprawdzamy przy pomocy jednostek.

Przykład Przykład 1.
75Przykład Przykład 2.
76Przykład Przykład 3.
79Przykład Przykład 4.
81Przykład Przykład 5.
83Przykład Przykład 6.
84Zadanie 8.1.3.
86Zadanie 8.1.4.
87Zadanie 8.1.5.
87Zadanie 8.1.6.
87Zadanie 8.1.8.
88Zadanie 8.1.9.
89Zadanie 8.1.10.
89Zadanie 8.1.15.
90Zadanie 8.1.21.
91Zadanie 8.1.24.
91Zadanie 8.1.25.
92Zadanie 8.1.28.
92Zadanie 8.1.30.
93Zadanie 8.1.33.
93Przykład Przykład 1.
94Przykład Przykład 2.
95Przykład Przykład 3.
97Zadanie 8.2.5.
99Zadanie 8.2.8.
100Zadanie 8.2.11.
100Zadanie 8.2.13.
100Zadanie 8.2.14.
101Zadanie 8.2.15.
101Przykład Przykład 3.
103Przykład Przykład 4.
106Zadanie 8.3.7.
108Zadanie 8.3.9.
109Zadanie 8.3.10.
109Zadanie 8.3.11.
109Przykład Przykład
110Zadanie 8.4.2.
112Przykład Przykład. Balon
116Zadanie Zadanie 1. Cykl przemian
118Zadanie Zadanie 2. Silnik spalinowy
118Zadanie Zadanie 3. Cząsteczki gazu
119
