W tym zadaniu oblicz objętość n = 3 moli gazu doskonałego w T = 27oC pod ciśnieniem normalnym p0 = 101325 Pa, jeśli n0 = 1 mol tego gazu w warunkach normalnych, tzn. w temperaturze T0 = 273 K i ciśnieniu normalnym, zajmuje objętość V0 = 22,4 dm3.
Zapisujemy równanie Clapeyrona dla stanu początkowego i końcowego, a następnie dzielimy równania stronami:
![]()
![]()
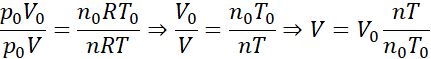
Podstawiając wartości liczbowe:
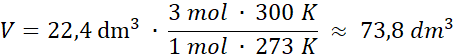
Odpowiedź: Gaz został ogrzany do temperatury około 196oC.

Zapisujemy równanie Clapeyrona dla stanu początkowego i końcowego, a następnie dzielimy równania stronami. Przeliczamy stopnie Celsjusza na kelwiny.

Przykład Przykład 1.
75Przykład Przykład 2.
76Przykład Przykład 3.
79Przykład Przykład 4.
81Przykład Przykład 5.
83Przykład Przykład 6.
84Zadanie 8.1.3.
86Zadanie 8.1.4.
87Zadanie 8.1.5.
87Zadanie 8.1.6.
87Zadanie 8.1.8.
88Zadanie 8.1.9.
89Zadanie 8.1.10.
89Zadanie 8.1.15.
90Zadanie 8.1.21.
91Zadanie 8.1.24.
91Zadanie 8.1.25.
92Zadanie 8.1.28.
92Zadanie 8.1.30.
93Zadanie 8.1.33.
93Przykład Przykład 1.
94Przykład Przykład 2.
95Przykład Przykład 3.
97Zadanie 8.2.5.
99Zadanie 8.2.8.
100Zadanie 8.2.11.
100Zadanie 8.2.13.
100Zadanie 8.2.14.
101Zadanie 8.2.15.
101Przykład Przykład 3.
103Przykład Przykład 4.
106Zadanie 8.3.7.
108Zadanie 8.3.9.
109Zadanie 8.3.10.
109Zadanie 8.3.11.
109Przykład Przykład
110Zadanie 8.4.2.
112Przykład Przykład. Balon
116Zadanie Zadanie 1. Cykl przemian
118Zadanie Zadanie 2. Silnik spalinowy
118Zadanie Zadanie 3. Cząsteczki gazu
119
