W tym zadaniu oblicz pracę uzyskaną w wyniku cyklu przemian n = 2 moli jednoatomowego gazu doskonałego przedstawionego na wykresie. Stan termodynamiczny gazu w punkcie (1) jest określony przez parametry p0 i V0, a jego temperatura wynosi T0 = 100 K. Znane są stała gazowa R, ciepło molowe gazu jednoatomowego przy stałej objętości ![]()
![]()

Praca w cyklu termodynamicznym jest równa polu wewnątrz cyklu na wykresie:
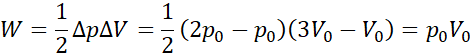
Z równania Clapeyrona dla stanu (1):
![]()
Podstawiając wartości liczbowe:
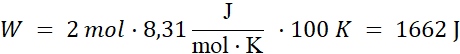
Odpowiedź: W wyniku cyklu uzyskano pracę 1662 J.

Praca użyteczna cyklu termodynamicznego jest równa polu figury wewnątrz cyklu w układzie współrzędnych (V, p). Korzystając z równania Clapeyrona przedstawiamy iloczyn ciśnienie i objętości jako iloczyn liczby moli, stałej gazowej i temperatury.

Przykład Przykład 1.
75Przykład Przykład 2.
76Przykład Przykład 3.
79Przykład Przykład 4.
81Przykład Przykład 5.
83Przykład Przykład 6.
84Zadanie 8.1.3.
86Zadanie 8.1.4.
87Zadanie 8.1.5.
87Zadanie 8.1.6.
87Zadanie 8.1.8.
88Zadanie 8.1.9.
89Zadanie 8.1.10.
89Zadanie 8.1.15.
90Zadanie 8.1.21.
91Zadanie 8.1.24.
91Zadanie 8.1.25.
92Zadanie 8.1.28.
92Zadanie 8.1.30.
93Zadanie 8.1.33.
93Przykład Przykład 1.
94Przykład Przykład 2.
95Przykład Przykład 3.
97Zadanie 8.2.5.
99Zadanie 8.2.8.
100Zadanie 8.2.11.
100Zadanie 8.2.13.
100Zadanie 8.2.14.
101Zadanie 8.2.15.
101Przykład Przykład 3.
103Przykład Przykład 4.
106Zadanie 8.3.7.
108Zadanie 8.3.9.
109Zadanie 8.3.10.
109Zadanie 8.3.11.
109Przykład Przykład
110Zadanie 8.4.2.
112Przykład Przykład. Balon
116Zadanie Zadanie 1. Cykl przemian
118Zadanie Zadanie 2. Silnik spalinowy
118Zadanie Zadanie 3. Cząsteczki gazu
119
