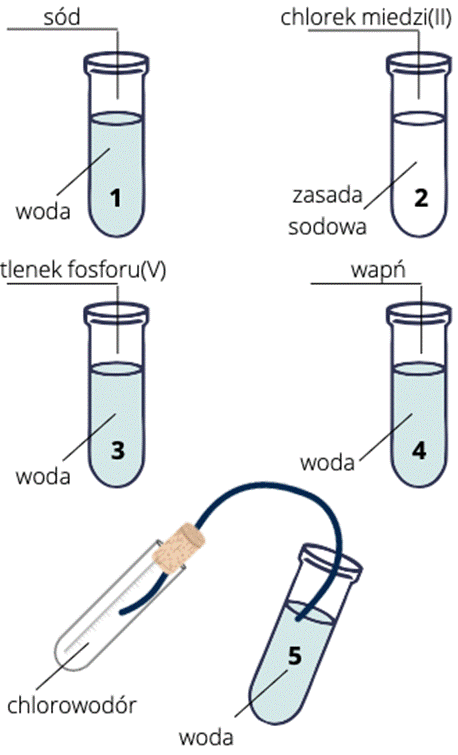
Sprzęt: pięć probówek, probówka z korkiem i wężykiem, uniwersalny papierek wskaźnikowy.
Odczynniki: woda, zasada sodowa, sód, wapń, tlenek fosforu(V), chlorowodór, chlorek miedzi(II).
Probówka 1:
Obserwacje: W probówce dochodzi do wydzielenia bezbarwnego, bezwonnego gazu. Uniwersalny papierek wskaźnikowy barwi się na niebiesko.
Wnioski: Powstał wodorotlenek sodu, a wydzielającym się gazem jest wodór.
Równanie reakcji: 2Na + H2O → 2NaOH + H2
Probówka 2:
Obserwacje: W probówce dochodzi do wytrącenia się niebieskiego, galaretowatego osadu.
Wnioski: Powstał wodorotlenek miedzi(II).
Równanie reakcji: CuCl2 +NaOH → Cu(OH)2 + 2NaCl
Probówka 3:
Obserwacje: Białe ciało stałe ulega rozpuszczeniu. Uniwersalny papierek wskaźnikowy barwi się na czerwono.
Wnioski: Tlenek fosforu(V) jest tlenkiem kwasotwórczym. W wyniku jego reakcji z wodą powstaje kwas fosforowy(V).
Równanie reakcji: P4O10 + 6H2O → 4H3PO4
Probówka 4:
Obserwacje: W probówce wytrąca się biały osad.
Wnioski: Powstał wodorotlenek wapnia.
Równanie reakcji: Ca + 2H2O → Ca(OH)2 + H2
Probówka 5:
Obserwacje: Po wpuszczeniu chlorowodoru do wody nie zachodzą widoczne oznaki reakcji. Po włożeniu uniwersalnego papierka wskaźnikowego do probówki dochodzi do jego zabarwienia na czerwono.
Wnioski: Powstał kwas chlorowodorowy.
HClg — woda → HClaq

Wodorotlenki grup 1 i 2 otrzymujemy przez kontakt metalu z wodą. W reakcji tej dochodzi dodatkowo do wydzielenia wodoru. W ten sposób możesz otrzymać między innymi wodorotlenek sodu czy wapnia. Wodorotlenki wyższych grup otrzymujemy w reakcji strąceniowej. W reakcji tej sól dobrze rozpuszczalna w wodzie reaguje z zasadą, w wyniku czego powstaje nierozpuszczalny wodorotlenek i inna rozpuszczalna sól. W ten sposób otrzymaj wodorotlenek miedzi(II) – skorzystaj z tablicy rozpuszczalności związków. Kwas fosforowy(V), tak jak wiele innych kwasów, możemy otrzymać w reakcji kwasowego tlenku (P4O10) z wodą. Kwas chlorowodorowy powstaje przez rozpuszczenie chlorowodoru w wodzie. Pamiętaj o uzgodnieniu równań reakcji.