W tym zadaniu oblicz temperaturę gazu składającego się z n1 = 55,63 moli azotu i n2 = 26,18 moli tlenu o łącznej objętości V = 10 l, jeśli jego energia wewnętrzna wynosi Ew = 0,5 MJ, wynik podaj w stopniach Celsjusza.
Energia wewnętrzna gazu jest średnią energią kinetyczną N dwuatomowych cząsteczek gazu:
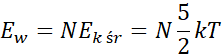
Liczba moli gazu w butli wyraża się zależnością:
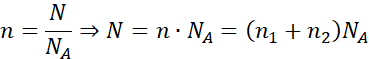
Więc:
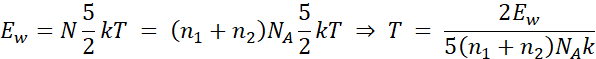
Podstawiając dane:
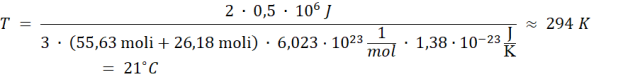
Odpowiedź: Gaz na temperaturę 21oC.

Azot i tlen są gazami dwuatomowymi, więc korzystamy ze wzoru na średnią energię kinetyczną dwuatomowej cząsteczki gazu, który pomnożony razy liczbę cząstek daje energię wewnętrzną gazu. Liczba moli jest ilorazem liczby cząsteczek i liczby Avogadra, skąd możemy obliczyć liczbę cząsteczek gazu. Przyjmujemy liczbę Avogadra ![]()
![]()

Przykład Przykład 1.
11Przykład Przykład 2.
12Przykład Przykład 3.
13Zadanie 7.1.2
14Zadanie 7.1.3
14Zadanie 7.1.5
15Zadanie 7.1.8
15Zadanie 7.1.9
15Przykład Przykład 1.
16Zadanie 7.2.1.
18Zadanie 7.2.3.
19Zadanie 7.2.12.
21Zadanie 7.2.13.
21Zadanie 7.3.2.
26Zadanie 7.4.1.
30Zadanie 7.4.11.
31Przykład Przykład 1.
32Przykład Przykład 3.
34Przykład Przykład 5.
37Zadanie 7.5.4.
38Zadanie 7.5.10.
39Zadanie 7.5.14.
40Zadanie 7.5.16.
40Zadanie 7.5.20.
41Zadanie 7.5.26.
42Przykład Przykład 1.
43Zadanie 7.6.2.
46Zadanie 7.6.6.
47Przykład Przykład 2.
49Zadanie 7.7.2.
52Zadanie 7.7.3.
52Zadanie 7.7.4.
53Zadanie 7.7.6.
53Przykład Przykład 1.
55Zadanie 7.8.7.
58Przykład Przykład. Gejzer
64Zadanie Zadanie 1. Śluza
66Zadanie Zadanie 2. Balon
67Zadanie Zadanie 3. Butla z gazem
67Zadanie Zadanie 4. Wartość energetyczna pożywienia
68
