

1. Aby rozwiązać tego typu zadania, musimy skorzystać z równania Clapeyrona. Równanie to obrazuje zależności między ilością gazu (w molach), objętością a warunkami (ciśnieniem i temperaturą):
p ∙ V = n ∙ R ∙ T, gdzie:
n — liczba moli gazu
P — ciśnienie [hPa]
V — objętość [dm3]
R — stała gazowa
T — temperatura [K]
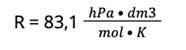
2. Metry sześcienne należy przeliczyć na decymetry sześcienne (0,01 m3 CO2 = 10 dm3 CO2).
3. 1 mol gazu w zajmuje 22,4 dm3. Dzięki temu możemy obliczyć, ile moli jest w 10 dm3 dwutlenku węgla.
22,4 dm3 – 1 mol
10 dm3 – x
x = 10 ∙ 1 : 22,4 = 0,45 [mol]
4. Wszystkie dane podstawiamy do równania i rozwiązujemy je.
pV = nRT
1020 ∙ V = 0,02 ∙ 0,45 ∙ 295
1020 ∙ V = 11031,5 / : 1020
V = 10,81 [dm3]