

1. Aby rozwiązać tego typu zadania, musimy skorzystać z równania Clapeyrona. Równanie to obrazuje zależności między ilością gazu (w molach), objętością a warunkami (ciśnieniem i temperaturą):
p ∙ V = n ∙ R ∙ T, gdzie:
n — liczba moli gazu
P — ciśnienie [hPa]
V — objętość [dm3]
R — stała gazowa
T — temperatura [K]
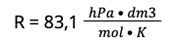
2. Musimy dopasować jednostki do tych, które potrzebne są we wzorze. Stąd temperaturę w stopniach Celsjusza należy przeliczyć na temperaturę w Kelwinach (0 stopni Celsjusza = 273 K). Ciśnienie należy przeliczyć na hPa (1 Pa = 0,01 hPa)
T = 15°C = 288 K
p = 101000 Pa = 1010 hPa
3. Wszystkie dane podstawiamy do wzoru i rozwiązujemy równanie.
pV = nRT
1010 ∙ V = 3 ∙ 83,1 ∙ 288
1010 ∙ V = 71798,4 | : 1010
V = 71,09 [dm3]